Osmosis
Osmosis adalah berpindahnya partikel pelarut dari larutan encer ke dalam larutan yang lebih pekat melalui selaput semipermiabel. Selaput semipermeabel hanya dapat dilalui oleh partikel pelarut dan tidak dapat dilalui oleh partikel terlarut.
Tekanan osmotik adalah tekanan hidrostatik yang terbentuk pada larutan akibat proses osmosis pelarut ke dalam larutan melalui membran semipermeabel. Selain itu, tekanan osmosis juga dapat didefinisikan sebagai tekanan luar yang diberikan pada larutan untuk menghentikan proses osmosis pelarut ke dalam larutan melalui membran semipermeabel. Jadi tekanan osmosis suatu larutan dapat berupa tekanan hidrostatis yang terbentuk di dalam larutan itu sendiri atau tekanan luar yang diberikan pada larutan tersebut untuk menghentikan proses osmosis.

Ada 3 jenis istilah jika kita bandingkan tekanan osmotik suatu larutan dengan larutan lainnya, yaitu:
- Isotonik, larutan yang mempunyai tekanan osmotik sama dengan tekanan osmotik larutan lainnya
- Hipertonik, larutan yang mempunyai tekanan osmotik lebih besar dari tekanan osmotik larutan lainnya
- Hipotonik, larutan yang mempunyai tekanan osmotik lebih kecil dari tekanan osmotik yang lain.
Rumus dari tekanan osmotik adalah:
Di mana :
M = Molaritas Larutan
R = Tetapan Gas (0,082 L.atm/mol.K)
T = Suhu (Kelvin = K)
i = faktor Van't Hoff = (n-1)+1
n adalah jumlah ion dan adalah derajat ionisasi
- Larutan elektrolit kuat =1
- Larutan elektrolit lemah 0<<1
- Larutan non elektrolit =0
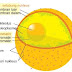
Osmosis adalah perpindahan molekul dari larutan berkonsentrasi rendah (hipotonis) menuju konsentrasi tinggi (hipertonis) melalui membran semipermeabel). Kondisi akhir dari peristiwa osmosis adalah diperoleh larutan isotonis. Isotonis adalah konsentrasi yang sama untuk dua larutan. Walaupun hasil akhirnya nanti akan memiliki volume yang berbeda.
Perhatikan gambar yang menunjukkan peristiwa osmosis di atas. Larutan pada bagian X merupakan hipotonik dan larutan Y merupakan hipertonik. Kondisi terserbut akan membuat larutan X berkurang dan menuju ke Y melalui M (membran semi permeabel).
Terdapat beberapa faktor yang mempengaruhi peristiwa osmosis. Beberapa faktor yang mempengaruhi osmosis antara lain adalah sebagai berikut.
- Ukuran molekul: semakin kecil ukuran molekul maka semakin cepat melewati membran sel.
- Luas permukaan: Jika luas permukaan membran sel semakin luas maka semakin besar proses atau daya serap membran sel tersebut.
- Ketebalan membran: membran yang tipis akan lenih memudahkan proses perpindahan larutan sehingga osmosis jauh lebih cepat.
- Tingkat larutan: molekul dengan tingkat kelarutan tinggi akan jauh lebih mudah untuk berpindah dibanding molekul yang tingkat kelarutannya rendah.
- Suhu: semakin tinggi suhu maka proses penyerapan zat akan semakin cepat.
Contoh peristiwa osmosis terjadi pada:
- Proses pemasangan infus pada pasien
- Penyerapan air dan unsur hara dari dalam tanah oleh rambut akar
- Pemberian garam pada sayur dan buah sehingga sayur dan buah menjadi lemas atau layu
- Mengerutnya sel darah merah yang dimasukkan ke dalam larutan hipertonis








Tidak ada komentar:
Posting Komentar